研究成果有体物(MTA)、臨床研究データ
研究成果有体物について
教職員等が本学において職務上又は本学の設備等を使用して得た研究成果有体物(マテリアル)の所有権は、原則として本学に帰属します。
【参照】「国立大学法人大阪大学研究成果有体物規程」
MTAについて
1.マテリアルを学外に提供する場合
マテリアルを企業・他機関等に提供する場合※1、「研究成果有体物移転契約(Material Transfer Agreement(MTA))」の締結が必要です。
- 1:研究者の異動に伴う、異動先へのマテリアル移転も含みます。
手続きの流れ
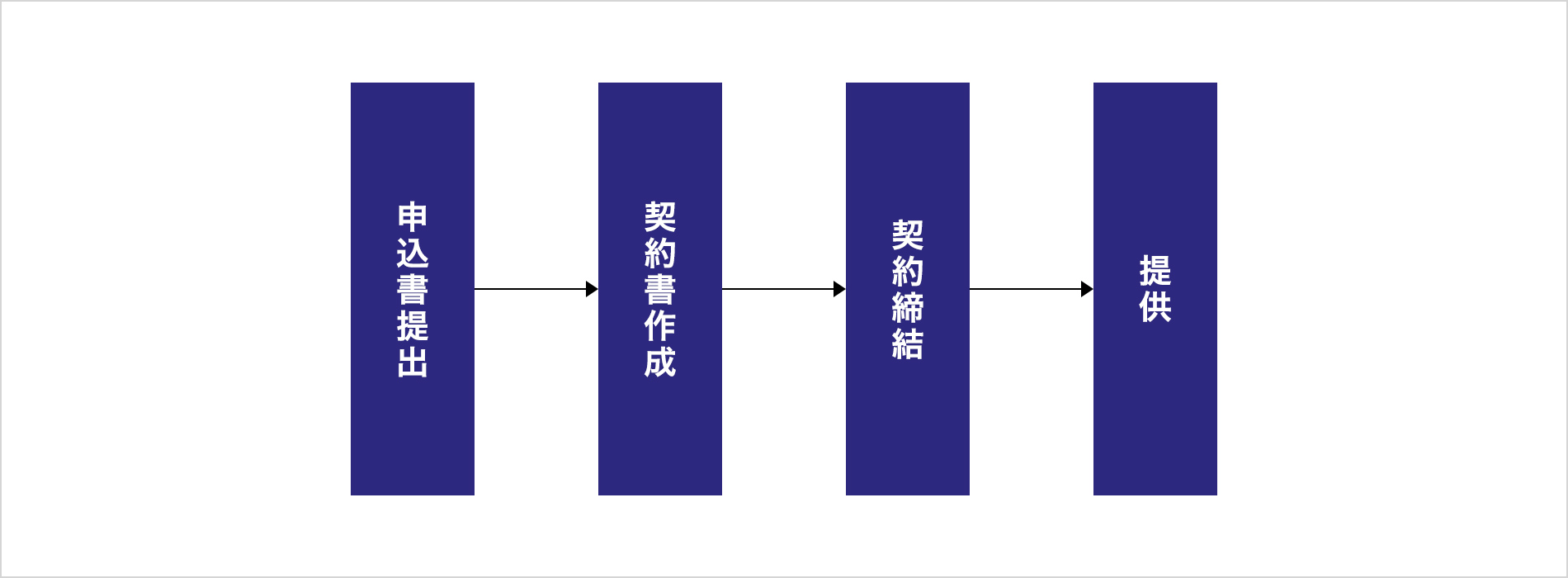
「研究成果有体物(提供)手続き申込書(エクセル)」を、下記アドレスまでお送りください。
mta-sec[at]uic.osaka-u.ac.jp
- メールアドレスの[at]は@に変換してください
2.学外マテリアルを導入する場合
MTAを求められた場合、提供機関の契約ひな型を使用し、企業・他機関等の指示に従い手続きをお願いします。基本的に研究代表者の署名で締結できます。
ご希望に応じてMTAの内容確認を知的財産室で担当します。
MTAに関する手続きの詳細は以下をご確認ください。
【参照】「研究成果有体物 手続き手順書」
【参照】規程・様式一式
「研究成果有体物(マテリアル)」
お問合せ先
共創機構イノベーション戦略部門知的財産室
MTA担当
mta-sec[at]uic.osaka-u.ac.jp または ipm[at]uic.osaka-u.ac.jp
- メールアドレスの[at]は@に変換してください
臨床研究データについて
臨床研究データ
臨床研究等により得られたデータその他の記録等並びに当該臨床研究等に基づき創作した全ての資料その他一切の学術及び産業上財産的価値のある成果(発明規程または研究成果有体物規程で適用されるもの以外)をいいます。
臨床研究等
被験者に対する治療薬、治験機器、治験製品、医薬品等の使用、手術、手技、診療行為等のうち、次のいずれかに該当するものをいいます。
1)医師主導治験
2)特定臨床研究
3)観察研究
4)介入研究等の臨床研究
5)上記の実施、薬事申請等に必要な非臨床試験
手続きの流れ
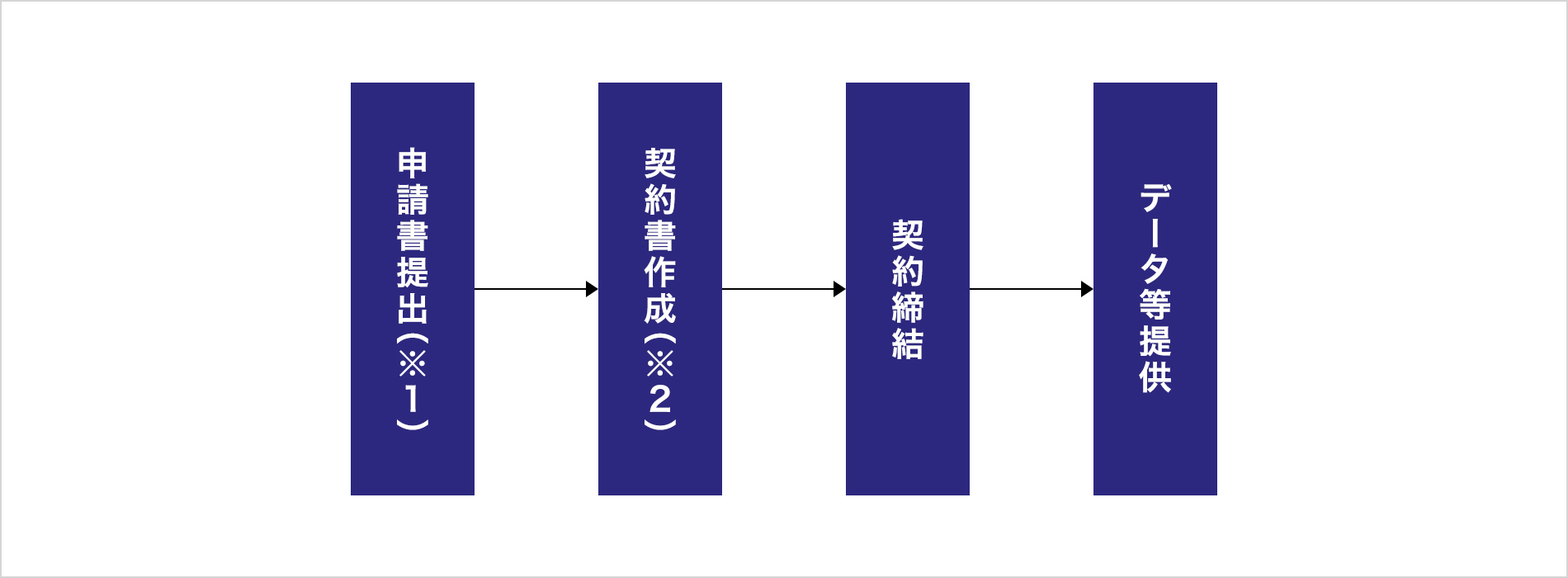
- 1: 自ら臨床研究等を実施する者又は研究責任者
- 2: 臨床試験データ移転および使用許諾契約書
【参照】「臨床研究データ利用許諾等規程」、「臨床研究データ利用許諾等申請書」
お問合せ先
共創機構イノベーション戦略部門知的財産室
ipm[at]uic.osaka-u.ac.jp
- メールアドレスの[at]は@に変換してください